瞄準生物製藥“卡脖子”難題,寶濟藥業(02659)給出技術驅動高質量發展答案
时间:2026-04-09 13:35:43
宝济药业-B
之前關注的多是ADC、雙抗等BD出海預期強的管線/公司,非腫管線看的不多。目前腫瘤賽道愈發擁擠,國內非腫創新項目佔比明顯升高,意味着我也必須將能力圈拓展至非腫管線。
恰好日前家裏侄子入職了上海一家叫寶濟藥業(02659)的公司,在替侄子“排雷”的同時順便翻了下寶濟藥業的資料。既然翻都翻了,就順便同步給大家,權當多個素材了。
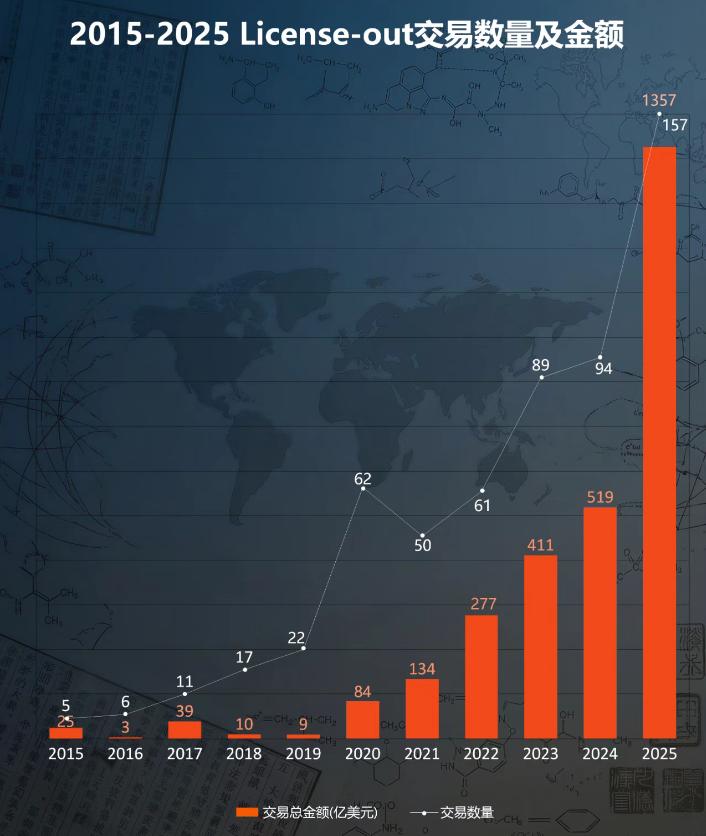
01 “量升”到“質變”,我國創新藥行業迎來“價值重估”
2025是我國創新藥里程碑式的一年。國家藥監局數據顯示,2025年我國達成創新藥BD出海157起,首付款70億美元,交易總金額1356.55億美元,遠超2024年94筆交易和519億美元的交易規模。
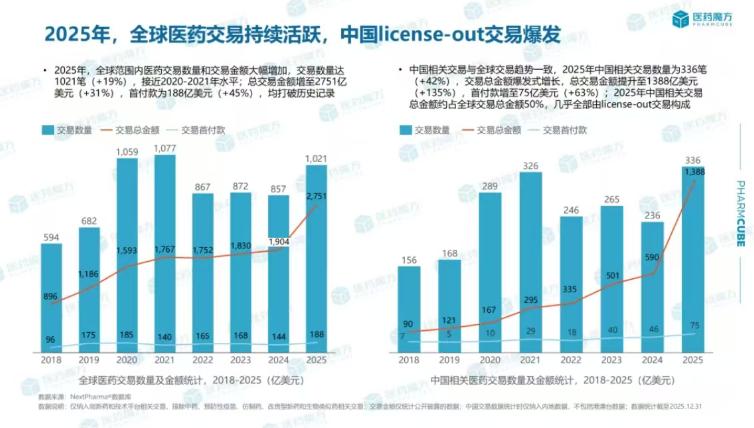
(醫藥魔方)
據醫藥魔方統計,我國去年創新藥BD金額佔全球總量的49%,首次超越美國成為全球創新藥第一大“發源地”。
2026年Q1我國創新藥企BD總金額再超600億美元。國內創新管線“好藥賤賣”一去不復返!
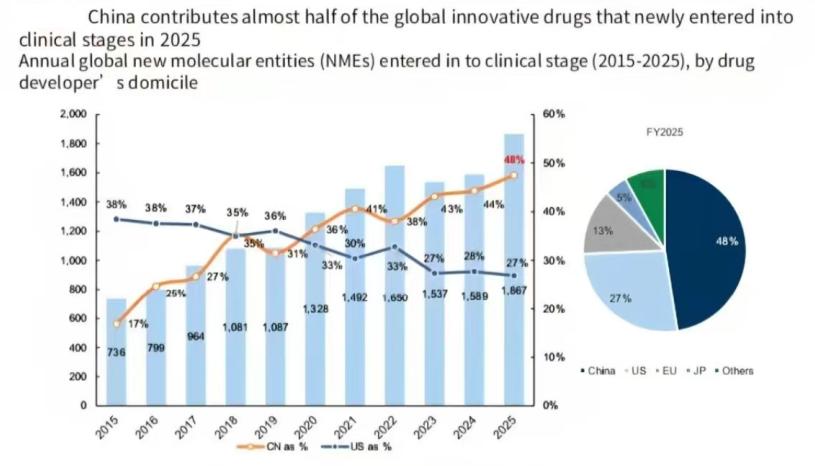
(高盛)
高盛統計數據顯示,我國藥企在研管線數量佔比升至全球48%,繼續鞏固着全球頭名的位置。
創新藥行業正不可避免地迎來價值重估。2025、2026以來(截至4月2日收盤)中證香港創新藥指數分別上漲56.8%和7.13%。近兩年個人長持的港股創新藥標的中,股價翻倍的不在少數。
02 生物製品利好政策紛至沓來,寶濟藥業致力於填補市場未被滿足的需求,解決“卡脖子”風險
近年,我國將關鍵生物製品自主可控視為國家競爭力的一部分,寶濟藥業主營的生物製藥利好政策不斷。2022年發佈的《“十四五”生物經濟發展規劃》提出要加快推進生物科技創新和產業化應用,打造國家生物技術戰略科技力量,提升產業鏈供應鏈安全穩定水平。《生物製造產業高質量發展行動計劃(2023-2027)》提出要重點突破一批“卡脖子”技術。今年3月出台的“十五五”規劃更是將生物製造與量子科技、核聚變同列七大未來產業之一……
寶濟藥業所在的上海市今年1月發佈了《支持現金製造業轉型升級三年行動方案(2026-2028年)》,將合成生物技術列為重點發展的先導產業。站在“自上而下”的角度分析,寶濟藥業所處的是永續、朝陽產業,又與上海市生物醫藥高質量發展的戰略定位吻合,若經營得當確實大有可為。

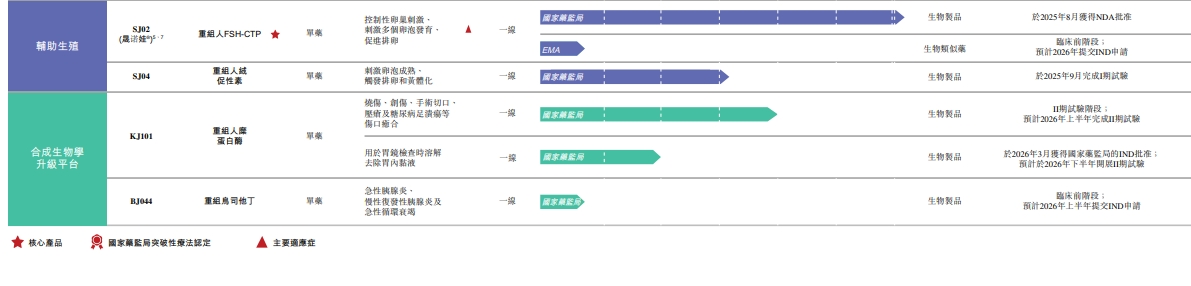
(寶濟藥業年報)
寶濟藥業現有12款在研管線,其中3款核心管線,另9款產品處於臨牀/臨牀前階段。
(一)KJ017
抗體等大分子藥物受限於分子量大、粘度高,難以通過皮下注射遞送,通常依賴靜脈注射。
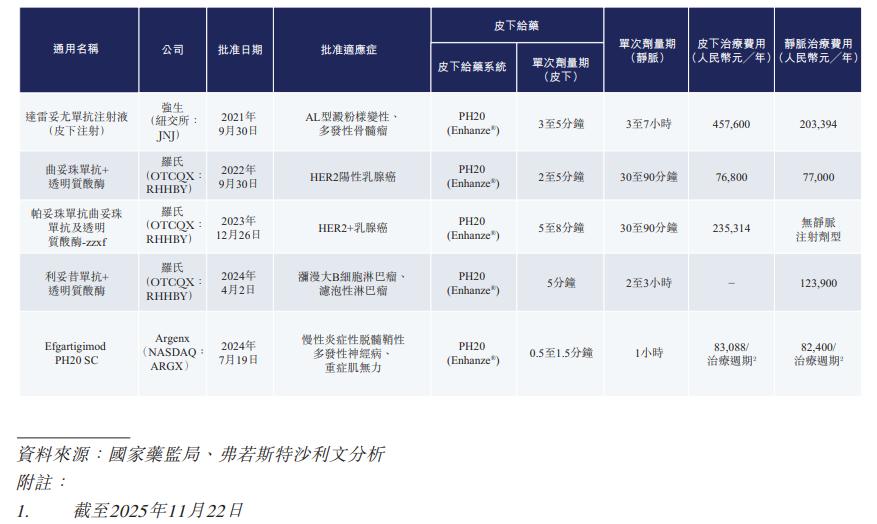
靜脈注射患者需前往醫療機構治療,靜脈注射時間通常在30-60分鐘之間。因個人體質差異,靜脈注射可能會導致過敏、支氣管痙攣、低血壓等輸注反映,部分抗體藥物相關不良反應發生率高達40%。而皮下注射不僅給藥時間縮短至10分鐘以內,藥物相關不良反應也僅限於輕度、短暫、局部。
重組人透明質酸酶可通過特異性降解組織中的透明質酸基質顯著提升藥物皮下滲透效率,讓大分子藥物也能實現皮下注射。
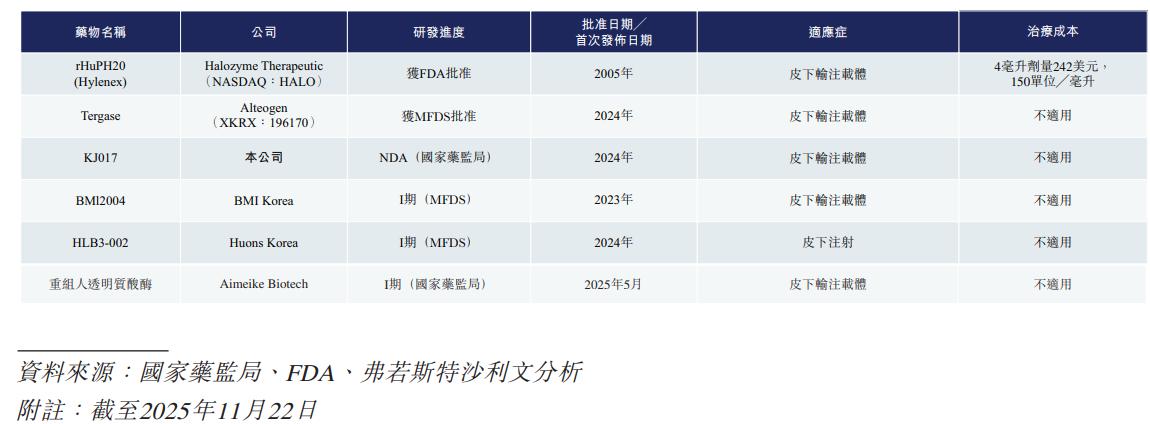
現全球獲批的重組人透明質酸酶有兩款,一是Halozyme的rHuPH20,二是韓國的Alteogen的Tergase。
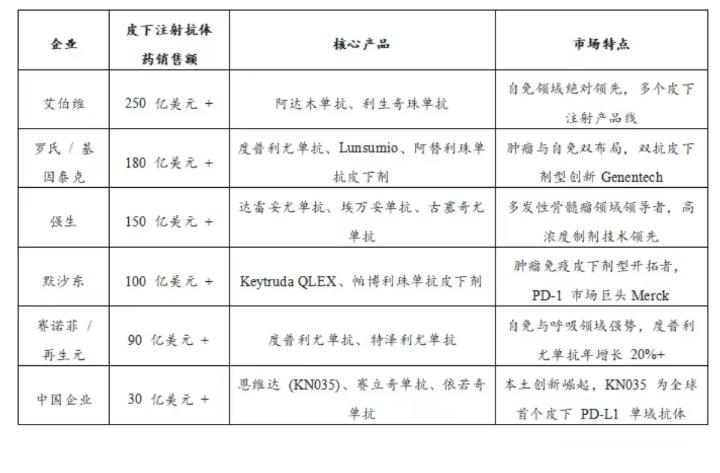
Halozyme將rHuPH20授權給羅氏、賽諾菲等MNC聯合開發的皮下注射抗體藥物年銷售額約800億美元。Halozyme將從銷售里程碑中穩定一筆穩定且不菲的收入。
今年1月20日,Alteogen與GSK子公司Tesaro簽署獨家許可,Tesaro獲得全球範圍內使用ALT-B4的權利以開發dostarlimab的皮下製劑,合作金額2.85億美元。3月25日,Alteogen又就ALT-B4與渤健達成獨家許可協議,共同推進皮下注射製劑的開發與商業化。Alteogen將獲得2000萬美元首付款及最高5.49億美元的里程碑付款,並在第二款產品啓動時額外獲得另外1000萬美元。
需要注意的是,rHuPH20和跨國藥企達成的是“靶點排他性”協議,易給我國藥企帶來“卡脖子”風險。如此來看,寶濟藥業KJ107的佈局極具戰略意義。
目前國內市場中,寶濟藥業的重組人透明質酸酶進展最快,KJ017已獲得國家藥監局的NDA批准,預計上半年獲批上市。友商宜明昂科在研的重組人透明質酸尚處I期臨牀。
生化藥品是從動物臟器、人體尿液等提取出的藥品,其生產過程整體制備工藝較為落後、藥品質量不穩定,生產工藝先天存在病毒、細菌污染風險,批次間質量差異大,難以從源頭杜絕各種微生物的污染和擴散。通過基因工程取代現有生化方式提取藥品的是保障人民羣眾用藥安全的必然要求。
寶濟藥業開發的重組透明質酸酶是利用基因工程取代動物臟器提取生化產品,實現了皮下注射而不產生過敏的跨越性進步。
寶濟藥業正積極推進KJ017的商業化推廣。現已與藥明生物、荃信生物、上海萊士、尚健等公司合作開發皮下製劑。另與處於不同階段的十餘家潛在合作伙伴制定業務發展計劃。
寶濟藥業同樣重視創新藥出海的機遇。現寶濟正計劃向歐洲藥品管理局和FDA提交KJ017的IND申請。
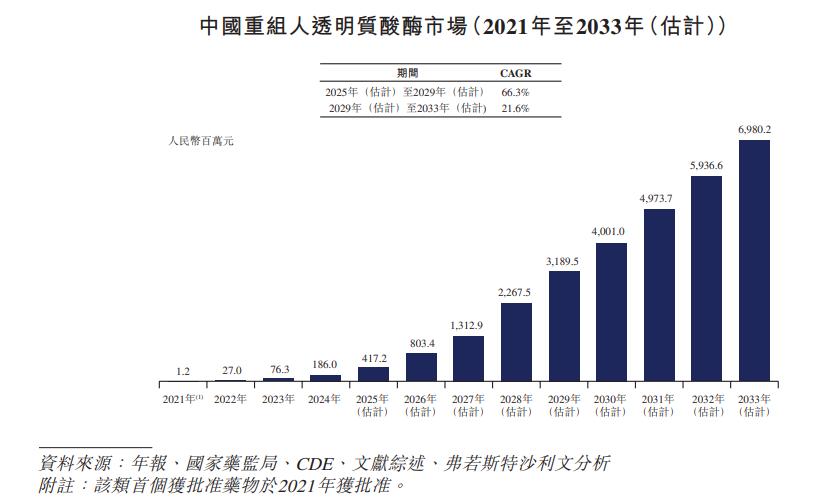
弗若斯特沙利文研究顯示,國內重組人透明質酸酶市場從2025年的4.17億元增至2030年的40.01億元,年化增速57.2%。料寶濟藥業將憑藉“國內首款”優勢分得增量市場中的大多數。
(二)KJ103
寶濟藥業的KJ103系全球唯一一款註冊臨牀階段的低免疫原性IgG降解酶。其腎臟移植前脱敏及抗腎小球基底膜(GBM)病適應症均獲得國家藥監局的突破性療法認定。
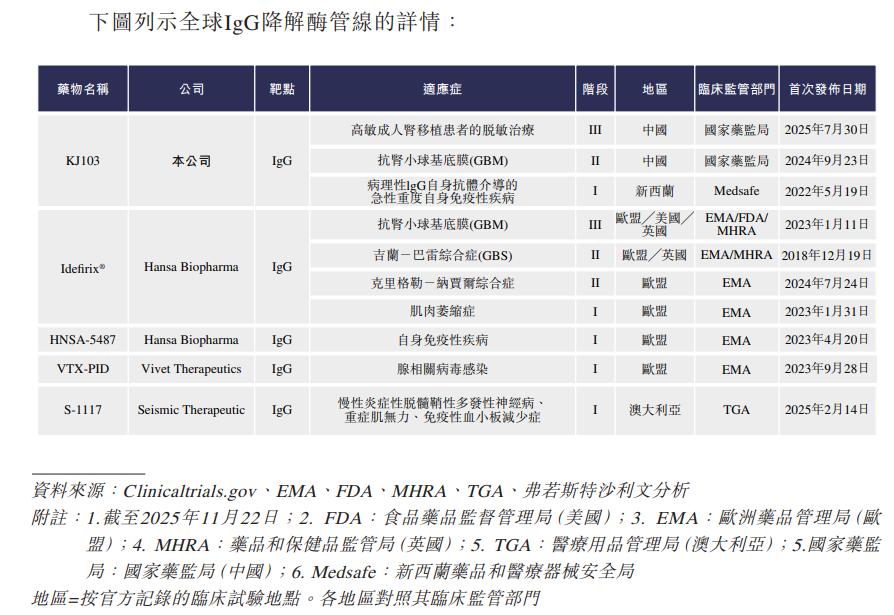
《中國器官捐獻和移植髮展報告(2024)》顯示,2024年我國共實施腎臟移植手術15387例,較2023年增長2.8%。去年我國腎臟移植約16000例。
國內部分中心披露信息顯示,完成腎移植的手術中高敏患者佔比約10%。美國器官資源共享網絡披露,等待腎移植的患者中,高敏患者佔比12%。目前我國等待腎移植的約15萬人。待KJ103成功獲批,將徹底解決國內部分患者無法移植的問題。KJ103腎臟移植前適應症已於今年3月完成III期試驗。
KJ103抗GBM病適應症預計2026年上半年啓動III期臨牀。II期臨牀研究顯示,KJ103給藥3個月後患者生存率為100%,其中66.7%的患者無需透析即可保留腎功能。治療6個月後整體生存率100%,75%的患者無需透析即可保留腎功能。而接受標準強化治療的GBM患者在給藥3.0個月後的整體存活率81.2%,其中僅30.6%的患者無需透析並可保留腎功能。KJ103該適應症具備BIC潛力。
一些投資者可能會認為KJ103適應症是罕見病,商業化想象空間不大。實際上我國近年來也正加強罕見病用藥的支持力度。2024年《在罕見疾病藥物臨牀研發中應用去中心化臨牀試驗的技術指導原則》、《以患者為中心的罕見疾病藥物研發試點工作計劃》發佈,不僅允許採用單臂試驗、真實世界證據等靈活研發方式,還將具有明顯臨牀價值的罕見病用藥/改良型新藥審評時限縮短至70日,並給予上市許可人較長的市場獨佔期。去年末我國有100餘種罕見病用藥納入國家醫保目錄,覆蓋超50種罕見病。今年國家衞健委披露的年度預算中,增設了“罕見病診療水平能力提升項目”新項目,預算7000萬元。
對於寶濟藥業這樣成立時間不長的創新藥企而言,拼PD-1或是聯合療法已經錯過了最佳時機。選擇罕見病用藥率先商業化與某些藥企通過小適應症突破是同一邏輯。況在政策支持下,罕見病用藥項目IRR並不低。
(三)SJ02
SJ02是寶濟藥業最先商業化的長效重組人卵泡刺激素羧基末端肽融合蛋白,用於輔助生殖領域。
弗若斯特沙利文發佈的《2026年中國輔助生殖行業發展現狀及未來趨勢白皮書》顯示,2025年我國輔助生殖滲透率已來到10.5%。中國不孕不育夫婦數量由2020年的5480萬對升至6060萬對,預計這一數字將在2035年升至7440萬對。
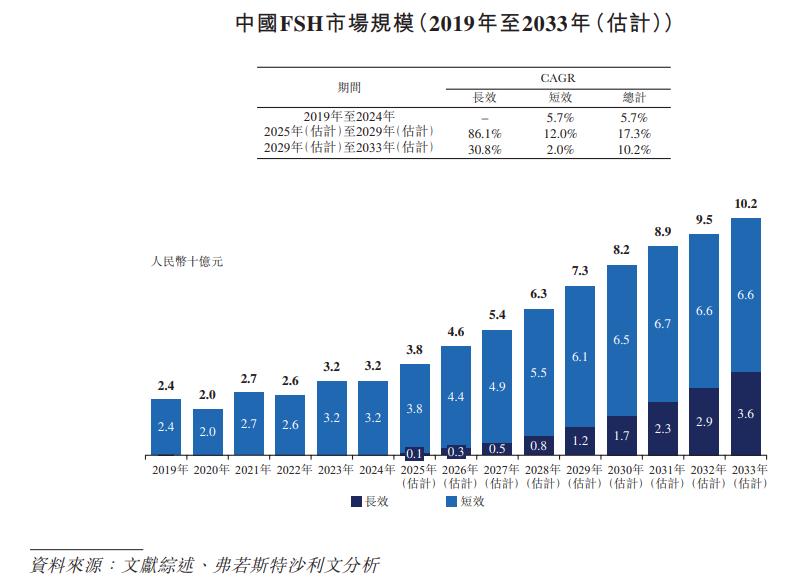
當前中國輔助生殖促排卵市場規模約46億元,基本由短效產品主導。SJ02上市後填補了國內長效促卵泡激素製劑的市場空白,為中國患者提供該領域國際同等質量的治療選擇。
去年7月,寶濟藥業與安科生物訂立獨家銷售代理協議,授予在後者在大中華區營銷、銷售、分銷及推廣SJ02的獨家權利。寶濟藥業去年11月交付了首批訂單。目前安科生物正推進SJ02入院及納入處方的程序。今年SJ02有望為寶濟藥業帶來千萬級增量收入。
(四)KJ101
寶濟藥業合成生物學平台可用於開發常規基因工程難以表達的重組藥物。其中KJ101(重組人糜蛋白酶)是寶濟轉入多個“伴侶蛋白基因”改造酵母工程細胞表達製備的重組人糜蛋白酶,可取代牛胰腺提取。具有純度更高、表達效率更高、生產流程更簡化及消除動物源性污染物風險。
KJ101燒傷、創傷、手術切口、褥瘡及糖尿病足潰瘍等適應症已在初步研究中已展現出顯著療效。現KJ101已完成II期臨牀入組。
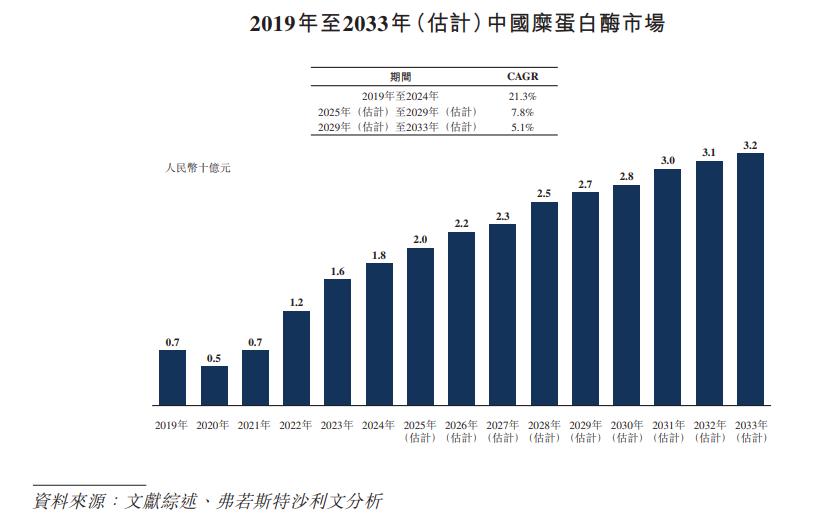
目前國內人糜蛋白酶的市場約20億。待寶濟藥業重組人糜蛋白酶上市後有望快速搶佔市場。
(五)BJ044
烏司他丁應用範圍涵蓋胰腺炎、手術後炎症、再灌注損傷、多器官功能障礙綜合徵、急性呼吸窘迫綜合徵等領域。
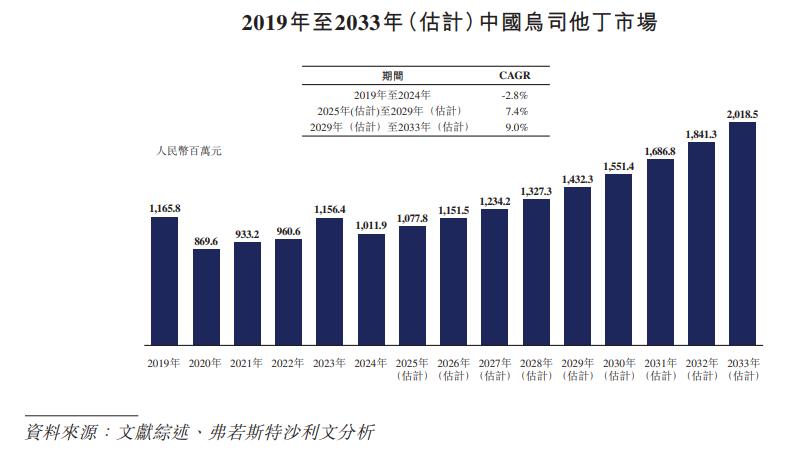
隨着人口老齡化加劇以及急慢性胰腺炎等免疫相關疾病發病率上升,烏司他丁市場規模將保持高個位數百分比增長。
BJ044(重組烏司他丁)是種小的循環蛋白多糖,存在於尿液、羊水中。重組人烏司他丁相較於烏司他丁製藥成本大幅降低,是生物製藥業高質量發展的新範式。寶濟藥業BJ044保留了其功能完整性及生理活性,並有望憑藉成本、可及性等優勢逐步替代烏司他丁。
寶濟藥業上述兩個品種均為全球首家開發的基因重組取代生化提取的具有廣泛臨牀應用價值的“重磅炸彈”。寶濟藥業已形成多平台、多適應症、國內+海外的多元商業化模式,是抗風險能力較強的Biotech!
03 “偶發性”開支盡皆靴子落地,寶濟生物或迎來商業化起勢年
去年寶濟藥業取得KJ017許可收入和SJ02商業化分成收入,營業收入由2024年的616萬元增至4915.6萬元。
KJ017大概率今年上半年獲批。考慮到2024年FDA批准的超34種高濃度抗體藥物中,皮下注射劑型佔比76%,且超90%的患者更樂於選擇皮下給藥。國內重組人透明質酸酶市場空間廣闊。KJ017補液/輔助皮下補液適應症與藥企擴大合作將助推寶濟藥業迫近盈虧平衡。
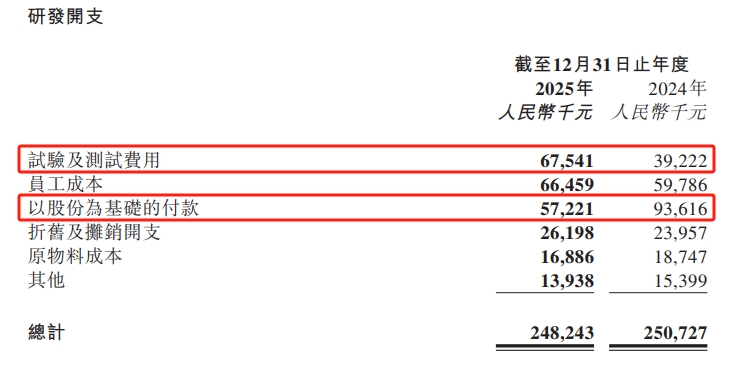
(寶濟藥業年報)
寶濟藥業在研創新管線大多是非腫項目,即使眾多項目同時在組,研發費用也相對可控。2025年寶濟藥業研發投入2.48億元,較2024年少了200萬左右。是因為股權激勵費用同比減少了超3600萬元,寶濟去年真正投入臨牀的“試驗及測試費用”其實還增加了2800餘萬元。

(寶濟藥業年報)
寶濟藥業去年虧損3.95億,同比增多約3100萬,主要是受非經營因素影響。去年寶濟計提訴訟虧損5676萬元,外匯淨虧損750萬元。

(寶濟藥業年報)
此外寶濟上市開支還同比多增2000萬元。若刨除上述偶發開支,寶濟藥業經調淨利潤還是向好的。
現金流方面,寶濟藥業去年末有息負債3.124億元,其中1.14億元一年內償還。不過寶濟在手現金及現金等價物12.416億元,不存在償債風險。現寶濟藥業已市值在300億+,且已納入港股通,不排除公司啓動回A股IPO計劃從而進一步充實現金流。
由於寶濟藥業剛上市不久便被納入了港股通,在流動性改善利好推動下,公司市值一度飆到了600億港幣左右(截至4月2日為335億)。加之澤璟製藥、迪哲等創新藥企業在尚未商業化/商業化尚未成熟前就登陸資本市場,且創新藥景氣度回暖,寶濟主研的還是解決生物技術的“卡脖子”產品,可以持續關注。
本文轉載自“明大教主”,智通財經編輯:馮秋怡。
免责声明:本资讯不构成建议或操作邀约,市场有风险,投资需谨慎!


